近日,國際權(quán)威學術(shù)期刊Nature Communications以“Interfacial-confined coordination to single-atom nanotherapeutics”為題,在線報道了我校材料科學與工程學院李永生教授、牛德超教授研究團隊和化工學院段學志教授研究團隊在“界面限域配位構(gòu)建單原子納米治療劑”方面取得的研究進展。
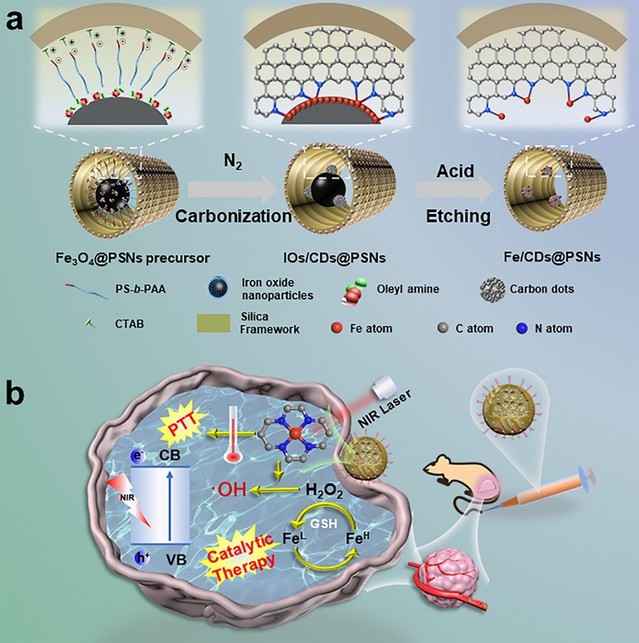
相較于大量關(guān)于碳基單原子體系在工業(yè)催化領(lǐng)域的研究,面向生物應(yīng)用的單原子材料的構(gòu)建仍處于起步階段。因此,發(fā)展高效的生物用單原子體系在生物醫(yī)藥領(lǐng)域具有重大的臨床應(yīng)用潛力。基于此,本工作提出了一種簡便通用的“界面限域配位”策略,在具有良好生物相容性的雙介孔二氧化硅孔道內(nèi)構(gòu)建金屬單原子納米治療劑用于腫瘤的高效安全治療。利用多孔氧化硅納米反應(yīng)器中的孔道限域效應(yīng),通過原位高溫碳化嵌段共聚物(聚苯乙烯-b-聚丙烯酸/PS-b-PAA)和含氮小分子(十六烷基三甲基溴化銨/CTAB和油胺)形成氮摻雜的碳點、再借助碳點與氧化鐵納米顆粒界面處的Fe-N-C配位作用及后續(xù)的酸刻蝕技術(shù),實現(xiàn)硅基Fe 單原子納米治療劑的可控精準構(gòu)筑。基于受限介孔孔道中獨特的Fe-N-C單原子結(jié)構(gòu),該硅基 Fe 單原子納米治療劑在外源性近紅外光輻照下具有高效的光熱轉(zhuǎn)換能力,其光熱轉(zhuǎn)換效率可達58.1%,是傳統(tǒng)碳基光熱試劑(不含單原子結(jié)構(gòu))的3倍之多。DFT計算進一步揭示了孔道限域環(huán)境下單原子結(jié)構(gòu)增強碳基材料光熱性能的內(nèi)在機制,主要源于孔道內(nèi)單原子錨定的缺陷碳結(jié)構(gòu)中電子密度增加、帶隙減小。此外,孔道中的Fe單原子結(jié)構(gòu)還具有pH/GSH雙觸發(fā)的腫瘤微環(huán)境響應(yīng)催化治療能力,即可將內(nèi)源性雙氧水轉(zhuǎn)化為羥基自由基來殺傷腫瘤細胞,并在細胞和活體層面分別論證了該硅基 Fe 單原子納米治療劑在高效腫瘤光熱/催化治療方面的應(yīng)用潛力。該工作將為設(shè)計和精準構(gòu)建具有可調(diào)變金屬成分的多功能單原子納米治療劑以實現(xiàn)安全有效的腫瘤治療提供了新的思路和科學指導。
我校材料科學與工程學院博士研究生秦利梅和化工學院博士研究生甘杰為該論文的共同第一作者,材料科學與工程學院李永生教授、牛德超教授和化工學院段學志教授為該論文的共同通訊作者。該研究還得到了中國科學院硅酸鹽研究所施劍林院士的悉心指導,上海光源姜政研究員和我校諾獎中心的戴升教授在同步輻射和球差電鏡表征方面給予大力支持。相關(guān)工作得到國家自然科學基金委創(chuàng)新群體和面上項目、上海市重大專項、上海市科委基礎(chǔ)重點項目以及上海市東方學者等項目資金的支持。
原文鏈接:https://www.nature.com/articles/s41467-021-27640-7