近日,我校材料科學(xué)與工程學(xué)院劉潤輝教授課題組在雙靶點(diǎn)抗耐藥真菌研究領(lǐng)域取得突破性進(jìn)展。耐藥真菌嚴(yán)重威脅人類生命健康,傳統(tǒng)的單靶點(diǎn)抗真菌藥物難以應(yīng)對耐藥真菌的迅速發(fā)展。雙靶點(diǎn)藥物有望通過作用于微生物的多個(gè)途徑顯著降低真菌耐藥發(fā)生,在藥物研究中具有很大前景。因此,設(shè)計(jì)和發(fā)現(xiàn)雙靶點(diǎn)抗耐藥真菌新分子對耐藥真菌感染治療和應(yīng)對真菌耐藥性挑戰(zhàn)具有重要意義。劉潤輝教授等研究人員首次成功設(shè)計(jì)并發(fā)現(xiàn)了具有高活性和高選擇性的雙靶點(diǎn)高效抗耐藥真菌新分子,解析了新分子通過真菌細(xì)胞膜和DNA雙靶點(diǎn)抗耐藥真菌機(jī)制,提出了雙靶點(diǎn)抗耐藥真菌活性分子的設(shè)計(jì)策略,為抗耐藥真菌藥物研究和應(yīng)對抗真菌耐藥性挑戰(zhàn)提供了新思路。研究成果以“A dual-targeting antifungal is effective against multi-drug resistant human fungal pathogens”為題發(fā)表在Nature Microbiology上(DOI:10.1038/s41564-024-01662-5)。這也是我校首次在微生物領(lǐng)域頂刊Nature Microbiology發(fā)表研究成果。
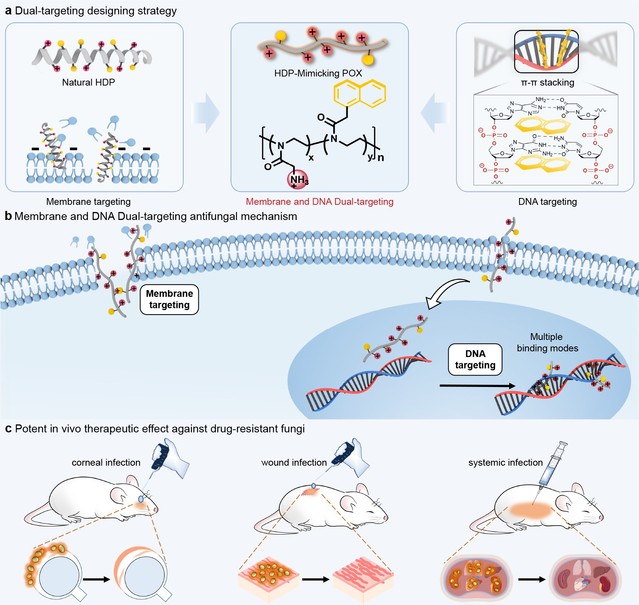
臨床抗真菌藥物數(shù)量有限且往往伴隨著嚴(yán)重的毒副作用,導(dǎo)致真菌感染對人類健康構(gòu)成重大威脅,真菌耐藥性的迅速出現(xiàn)和傳播加劇了這一現(xiàn)狀。雙靶點(diǎn)藥物有望通過作用于微生物的多個(gè)途徑顯著降低真菌耐藥發(fā)生,在藥物研究中具有很大前景。盡管臨床中通過兩種藥物聯(lián)用的替代方案實(shí)現(xiàn)雙靶點(diǎn)抗耐藥真菌,但兩種藥物在體內(nèi)的分布和藥代動力學(xué)各不相同,使得治療效果受到限制。真菌和哺乳動物細(xì)胞同作為真核細(xì)胞結(jié)構(gòu)高度相似,導(dǎo)致抗真菌靶點(diǎn)有限,即使發(fā)現(xiàn)單一靶點(diǎn)的選擇性抗真菌分子也極其困難。因此,雙靶點(diǎn)藥物在抗真菌研究領(lǐng)域一直未取得突破。劉潤輝教授課題組在前期研究中,提出了以優(yōu)異生物安全性的聚噁唑啉(多肽主鏈上酰胺鍵轉(zhuǎn)移至側(cè)鏈)模擬天然多肽,創(chuàng)新性地實(shí)現(xiàn)了基于聚噁唑啉骨架的功能性多肽模擬,發(fā)現(xiàn)了體內(nèi)外高效抗耐藥細(xì)菌和耐藥真菌的聚噁唑啉活性分子(Angew. Chem. Int. Ed.2020, 59, 6412,VIP論文,ESI高被引;Angew. Chem. Int. Ed. 2022, 61, e202200778,VIP論文;J. Am. Chem. Soc.2023, 145, 25753,JACS Spotlight)。本研究中進(jìn)一步提出通過正電荷和兩親性的聚噁唑啉模擬宿主防御肽同時(shí)引入DNA結(jié)合基團(tuán)作為疏水性結(jié)構(gòu)的設(shè)計(jì)策略,通過調(diào)控正電荷和DNA結(jié)合基團(tuán)的比例成功獲得了高活性、高選擇性雙靶點(diǎn)抗耐藥真菌新分子。雙靶點(diǎn)活性分子對多種臨床常見耐藥真菌(包括念珠菌屬、新生隱球菌、格特隱球菌和煙曲霉菌)具有高活性和高選擇性,在角膜炎、擦傷、系統(tǒng)感染等多個(gè)小鼠感染模型中展示優(yōu)異治療耐藥真菌感染效果,為抗耐藥真菌藥物研究和應(yīng)對抗真菌耐藥性挑戰(zhàn)提供了新思路。
我校副研究員周敏、博士研究生劉龍強(qiáng)是論文的第一作者,劉潤輝教授為通訊作者。該成果得到了國家自然科學(xué)基金委杰出青年科學(xué)基金、科技部重點(diǎn)研發(fā)項(xiàng)目等基金的資助。
論文鏈接: https://www.nature.com/articles/s41564-024-01662-5