近日,我校材料科學(xué)與工程學(xué)院劉昌勝院士團(tuán)隊(duì)在干細(xì)胞治療研究取得新進(jìn)展,相關(guān)研究成果以“In situ licensing of mesenchymal stem cell immunomodulatory function via BMP-2 induced developmental process”為題,于2024年11月20日發(fā)表在《美國國家科學(xué)院院刊》(PNAS)上。
間充質(zhì)干細(xì)胞(MSCs)因其卓越的免疫調(diào)節(jié)功能、低免疫原性和多向分化潛能,在克羅恩病、移植物抗宿主病、系統(tǒng)性紅斑狼瘡等多種炎癥性疾病的治療中具有重要價(jià)值。研究表明,當(dāng)MSCs被招募到炎癥部位時(shí),功能會(huì)受到周圍免疫細(xì)胞的影響,一般需通過炎癥因子預(yù)處理MSCs,以增強(qiáng)其免疫調(diào)節(jié)能力。但這種預(yù)處理會(huì)導(dǎo)致MSC失去免疫豁免權(quán),容易被宿主免疫系統(tǒng)清除,且預(yù)處理后的功能增強(qiáng)隨著時(shí)間延長逐漸下降,限制了其臨床應(yīng)用。
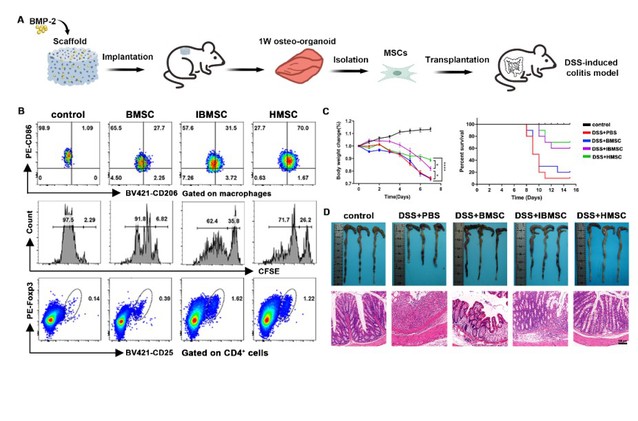
為解決這一問題,研究團(tuán)隊(duì)提出了一種新型的“自體MSC原位授權(quán)”策略,通過植入負(fù)載骨形態(tài)發(fā)生蛋白2(BMP-2)的生物活性材料在體內(nèi)構(gòu)建類骨組織,借助發(fā)育早期的炎性微環(huán)境來激活MSCs的免疫調(diào)節(jié)功能。研究表明,該方法所獲得的自體MSCs具有更低的免疫原性,有助于其在宿主中的長期存活,且更長時(shí)間保持其免疫調(diào)節(jié)能力。這些優(yōu)異的免疫調(diào)節(jié)特性使其在小鼠潰瘍性結(jié)腸炎的治療中獲得顯著的效果,降低死亡率,重塑結(jié)腸部位炎癥生態(tài)位。這種由植入活性材料而產(chǎn)生的自體來源MSC為干細(xì)胞治療提供了一種有前景的全新細(xì)胞來源。
我校材料科學(xué)與工程學(xué)院博士生朱富威為論文第一作者,我校王靖教授、劉昌勝教授為通訊作者。該研究工作得到了國家自然科學(xué)基金基礎(chǔ)科學(xué)中心項(xiàng)目、國家自然科學(xué)基金重點(diǎn)項(xiàng)目、材料生物學(xué)與動(dòng)態(tài)化學(xué)前沿科學(xué)中心和國家自然科學(xué)基金青年科學(xué)基金的支持。
原文連接:https://www.pnas.org/doi/10.1073/pnas.2410579121