近日,我校材料科學與工程學院李永生教授團隊在納米醫(yī)學腫瘤治療領(lǐng)域取得新進展,相關(guān)研究成果以“Tumor Microenvironment-Responsive Engineered Hybrid Nanomedicine for Photodynamic-Immunotherapy via Multi-Pronged Amplification of Reactive Oxygen Species”為題發(fā)表在《自然-通訊》(Nature Communications, 2025, 16, 424.)上。
基于活性氧(ROS)的腫瘤療法,如光動力療法、聲動力療法、化學動力學療法等已被廣泛研究。然而,細胞內(nèi)抗氧化應激防御機制由于可減輕腫瘤部位ROS的細胞毒性、幫助腫瘤細胞逃避氧化應激損傷,使ROS基療法治療水平大打折扣。近期提出的原位多途徑調(diào)控ROS策略有望在提高療效中發(fā)揮作用,但腫瘤細胞內(nèi)、外源ROS調(diào)控途徑之間往往會相互干擾,且腫瘤微環(huán)境(TME)內(nèi)存在的嚴重缺氧狀態(tài)又制約了其療效的發(fā)揮。因此,亟需發(fā)展針對腫瘤微環(huán)境中不同組分間相互作用的ROS調(diào)控策略,以放大腫瘤治療療效。成纖維細胞在TME中廣泛分布并且伴隨癌癥的進展會被誘導成激活狀態(tài)形成癌癥相關(guān)成纖維細胞 (CAFs),活化的CAFs將使腫瘤內(nèi)部產(chǎn)生高間充質(zhì)壓力,進而壓迫腫瘤血管、減少納米藥物滲透并阻礙外部氧氣供應導致治療效果不理想。基于此,研究團隊利用TME中的CAFs這一靶點,設計并構(gòu)建了一種新型TME響應雜化納米藥物(ZnPP@FQOS),其通過“限域”裝載原卟啉鋅(ZnPP)和槲皮素(Que),可實現(xiàn)CAFs的重塑以及內(nèi)、外源多途徑ROS的調(diào)控,進而增強腫瘤治療效果(圖1)。當ZnPP@FQOS經(jīng)血管滲入TME時,它首先會響應TME的弱酸性pH值從硅基雜化殼層中釋放Que,作用于CAFs并將其重塑,為ROS生成提供氧氣原料以緩解缺氧且有助于納米藥物滲透。同時,被腫瘤細胞內(nèi)吞的Que可通過下調(diào)凋亡拮抗蛋白Bcl-xL實現(xiàn)細胞凋亡。此外,進入腫瘤細胞后二硫鍵交聯(lián)的雜化硅基殼層會響應過量的谷胱甘肽釋放ZnPP,從而在激光照射時引發(fā)光動力效應產(chǎn)生單線態(tài)氧,并通過下調(diào)血紅素加氧酶1(HO-1)破壞抗氧化應激防御系統(tǒng),最終實現(xiàn)了內(nèi)、外源“多管齊下”的ROS調(diào)控策略。
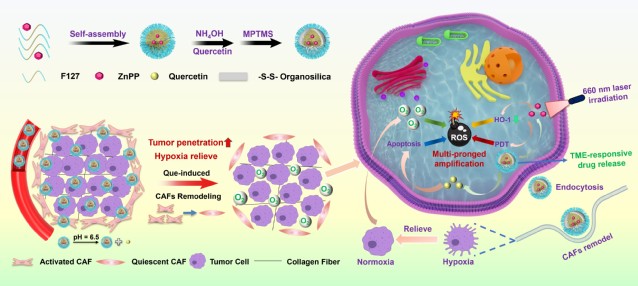
圖1. ZnPP@FQOS的制備流程及通過內(nèi)、外源“多管齊下”ROS調(diào)控以提高腫瘤療效的機理示意圖
研究團隊進一步在細胞及活體層面分別驗證了ZnPP@FQOS的深層組織穿透能力(圖2)。細胞層面上構(gòu)建了肺癌細胞(KP)與CAFs(3T3)共混的多細胞腫瘤球作為體外模型對納米藥物組織滲透能力進行評估,結(jié)果表明ZnPP@FQOS在弱酸性條件下能夠成功滲入平均直徑為120 μm的腫瘤球內(nèi)核,在70 μm處有較強熒光分布,具有良好滲透能力。活體層面上對淺層(0 mm)以及深層(3 mm)的腫瘤組織進行切片,并且對血管進行染色,發(fā)現(xiàn)ZnPP@FQOS相較于其他兩組藥物有明顯的深層組織熒光積累及更遠的血管滲透距離,說明該納米藥物具有良好的腫瘤組織滲透能力。
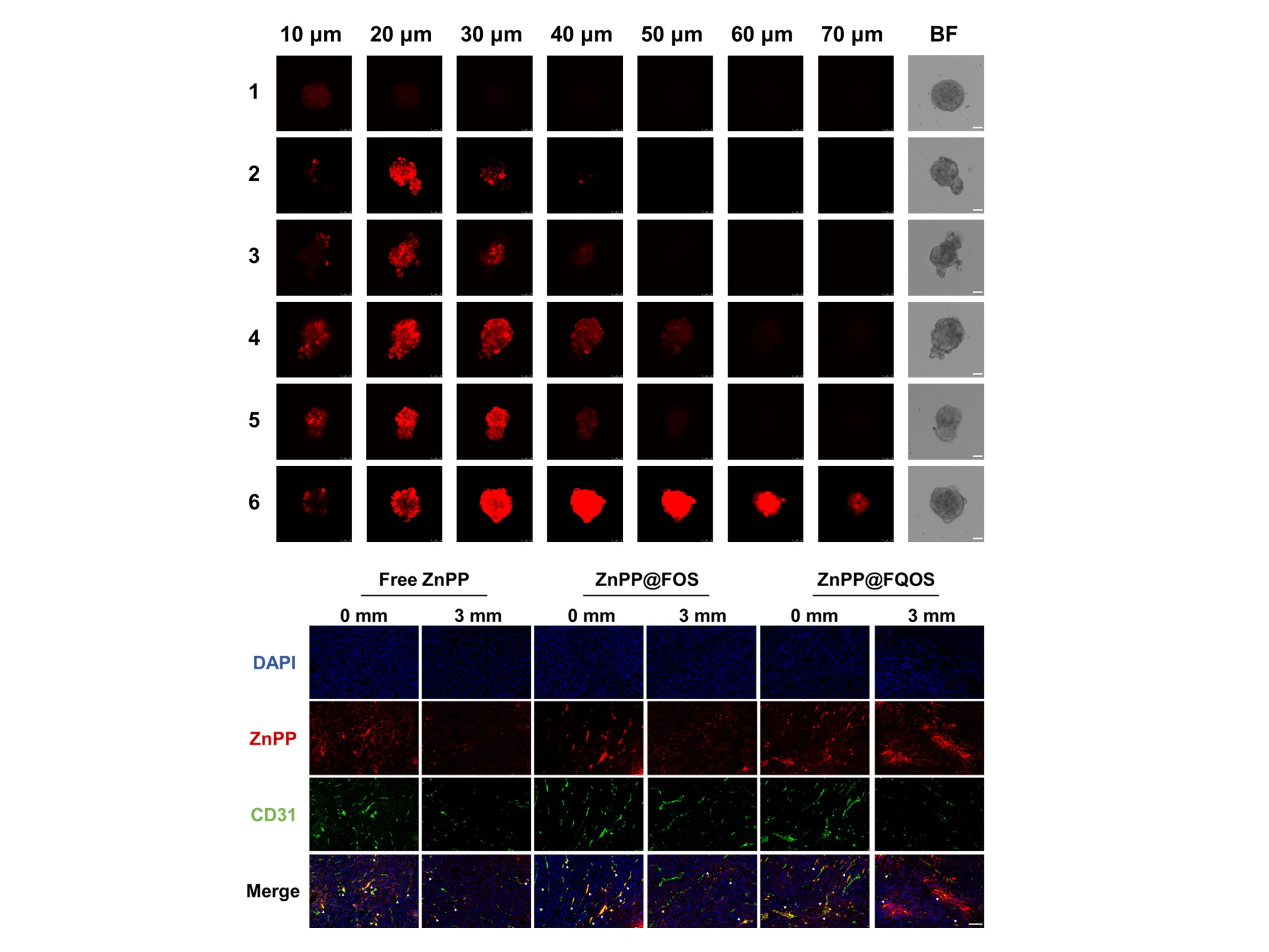
圖2. 利用多細胞腫瘤球以及腫瘤組織評估ZnPP@FQOS的組織滲透能力。(1:Free ZnPP; 2:ZnPP@FOS; 3:ZnPP@FOS pH=6.5; 4:ZnPP@FOS+Free Que; 5:ZnPP@FQOS; 6:ZnPP@FQOS pH=6.5)
通過建立荷瘤小鼠模型,研究團隊系統(tǒng)探究了ZnPP@FQOS的抑瘤效果及免疫應答激活能力(圖3)。基于KP肺癌皮下瘤模型發(fā)現(xiàn)其具有顯著的抑瘤效果,抑瘤率達到了92.9%;通過對腫瘤內(nèi)的ROS進行染色成功地在活體層面證明了內(nèi)、外源“多管齊下”ROS調(diào)控策略的成功實現(xiàn)。其次構(gòu)建了Pan02胰腺癌雙側(cè)腫瘤模型進一步驗證ZnPP@FQOS聯(lián)合免疫檢查點阻斷療法后的全身性免疫激活效果。結(jié)果表明,ZnPP@FQOS治療后脾臟中的成熟樹突狀細胞數(shù)量得到顯著提升,并且原發(fā)及遠端腫瘤經(jīng)納米藥物治療后的細胞毒性T細胞數(shù)量均大幅增加,說明其成功激活了小鼠的全身性免疫反應,扭轉(zhuǎn)了胰腺癌的嚴重抑制免疫微環(huán)境。該工作將為設計和精準構(gòu)建以ROS調(diào)控為基礎的納米藥物從而實現(xiàn)安全高效的腫瘤治療提供了新思路。
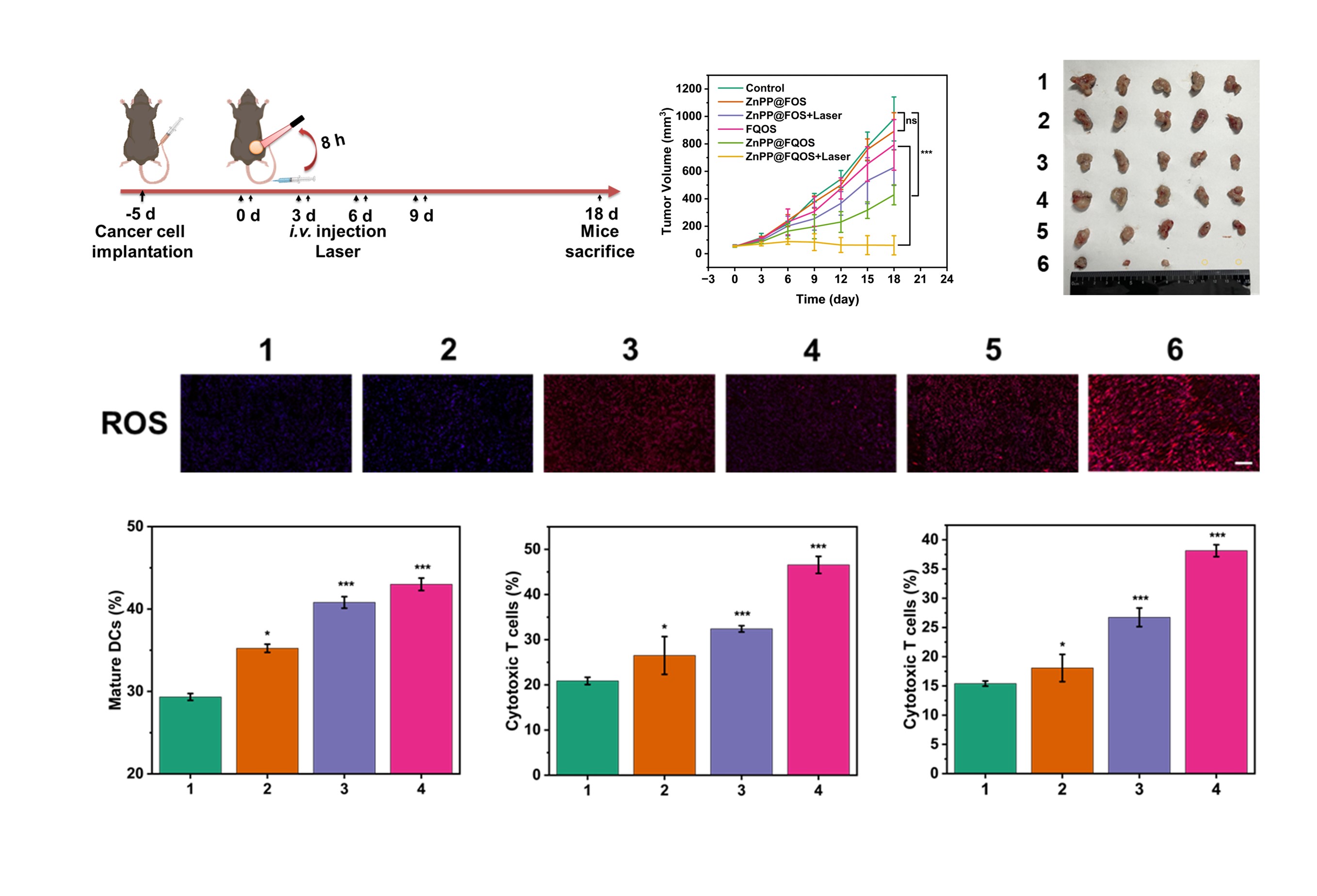
圖3. 單側(cè)及雙側(cè)皮下腫瘤模型模擬ZnPP@FQOS的抑瘤能力、ROS調(diào)控效果以及全身性免疫激活能力。單側(cè)瘤模型分組:(1:Control; 2:ZnPP@FOS; 3:ZnPP@FOS+Laser; 4:FQOS; 5:ZnPP@FQOS; 6:ZnPP@FQOS+Laser);雙側(cè)瘤模型分組:(1: Control; 2: Anti-PD-L1; 3: ZnPP@FQOS+Laser; 4: ZnPP@FQOS+Laser+anti-PD-L1)
我校材料科學與工程學院博士研究生鄒鏡霖為論文第一作者,上海市肺科醫(yī)院姜聰、胡強勝博士為共同第一作者。我校李永生教授、上海市肺科醫(yī)院張鵬教授為共同通訊作者。該研究工作得到了國家重點研發(fā)計劃、國家自然科學基金、上海領(lǐng)軍人才等項目的支持。
論文鏈接:https://www.nature.com/articles/s41467-024-55658-0