近日,我校材料科學(xué)與工程學(xué)院劉昌勝院士/俞遠(yuǎn)滿副教授團(tuán)隊(duì)在Science Advances發(fā)表了文章Inflamed vessel-anchored release of H2 across the blood-brain barrier for ischemic stroke neuroprotection。該研究構(gòu)建了一種選擇性血管錨定的氫分子(H?)釋放平臺(tái),無(wú)需納米顆粒穿透血腦屏障即可為缺血性腦卒中提供卓越的神經(jīng)保護(hù)作用,并被選為當(dāng)期Featured Article。
與傳統(tǒng)藥物分子相比,H?具有多種顯著優(yōu)勢(shì),例如極佳的血腦屏障滲透性、快速的組織分布、高生物安全性以及抗氧化和免疫調(diào)節(jié)作用。然而,由于其快速擴(kuò)散和缺乏靶向性,無(wú)論是靜脈/口服富氫水還是吸入氫氣都無(wú)法在病灶處維持高濃度的氫分子,這極大地限制了氫分子療法的療效。目前,如何在腦卒中病灶部位實(shí)現(xiàn)持續(xù)的氫氣釋放而不導(dǎo)致顱內(nèi)納米顆粒積聚仍是一個(gè)難題。本研究通過與P-選擇素結(jié)合肽修飾的ZrSi2納米顆粒(ZSNP),開發(fā)了一種針對(duì)炎癥血管的錨定型產(chǎn)氫系統(tǒng)。該設(shè)計(jì)可在不穿透血腦屏障的基礎(chǔ)上,通過水解在穩(wěn)定長(zhǎng)周期持續(xù)產(chǎn)生H2,并且不會(huì)引發(fā)明顯的pH波動(dòng)。
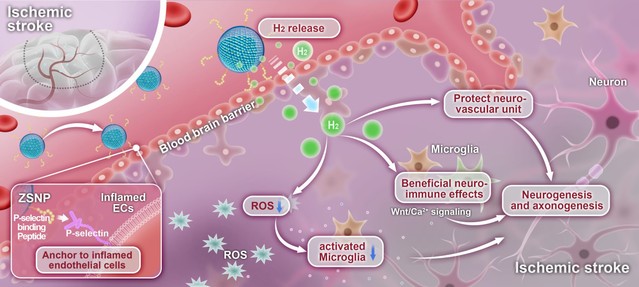
在機(jī)制層面,ZSNP能夠促進(jìn)小膠質(zhì)細(xì)胞介導(dǎo)的血管生成和神經(jīng)發(fā)生,引導(dǎo)軸突沿著新生血管的軌跡向梗死區(qū)域生長(zhǎng),并通過非經(jīng)典的Wnt/Ca2?信號(hào)通路促進(jìn)小膠質(zhì)細(xì)胞與神經(jīng)元之間的相互作用。這種神經(jīng)血管網(wǎng)絡(luò)的重建有助于功能神經(jīng)回路的重新整合,從而實(shí)現(xiàn)結(jié)構(gòu)和功能的恢復(fù),其效果優(yōu)于臨床藥物依達(dá)拉奉。并且在長(zhǎng)周期(術(shù)后12周)的治療過程中,凸顯出了明顯的促神經(jīng)功能恢復(fù)能力。該策略為缺血性腦卒中提供了一種有前景且負(fù)擔(dān)較低的神經(jīng)保護(hù)方法。
本校俞遠(yuǎn)滿副教授,中國(guó)科學(xué)院深圳先進(jìn)技術(shù)研究院范明儉博士后為共同第一作者;華東理工大學(xué)劉昌勝院士,中國(guó)科學(xué)院深圳先進(jìn)技術(shù)研究院唐為研究員/李光林研究員,上海交通大學(xué)何前軍教授為共同通訊作者。
論文鏈接: https://www.science.org/doi/10.1126/sciadv.aea3355